Пересадка органов (или тканей) является стандартной клинической процедурой. Однако, в связи с тем что человечество стремительно стареет, а методы, позволяющие бороться с отторжением трансплантатов, совершенствуются, потребность в пересадке органов превосходит количество донорских органов.
Иммунология пересадки органов
Существует 4 вида трансплантации.
- Аутопластика. Ткани трансплантируются с одной части тела человека на другую (например, кожа со спины пересаживается на лицо).
- Изотрансплантация. Между генетически идентичными людьми (например, пересадка почек между однояйцевыми близнецами). В данном случае не возникает иммунологических осложнений (отторжения) и трансплантат принимается организмом рецепиента.
- Аллопластика. Пересадка органов или тканей в пределах одного биологического вида (например, от человека к человеку). Это обычный вариант трансплантации.
- Ксеногшастика. Между различными биологическими видами (например, пересадка свиного сердца человеку). В этих случаях организм при восприятии трансплантата как чужеродного отторгает его.
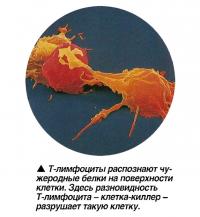
Чужеродные органы
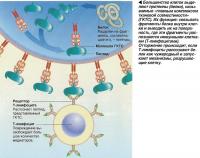
Мигрирующие клетки иммунной системы реципиента, лимфоциты Т-хелперы (от английского helper - помощник), распознают «новые» клетки пересаженного органа и воспринимают их как чужеродные из-за того, что на их поверхности (клеточной мембране) находится ряд белков, называемых антигенами, нетипичных для организма реципиента. Механизм распознавания запускается группой протеинов (специализированных белков) - главного комплекса тканевой совместимости клетки (ГКТС), который дает иммунной клетке сигнал к уничтожению «чужого» антигена; таким образом включается механизм отторжения донорских органов и тканей.
Отторжение
Клетки Т-хелперы запускают в организме процессы, которые приводят к разрушению или отторжению трансплантата. Выделяются медиаторы (от латинского mediator - посредник), физиологически активные вещества, гормоны или белки, благодаря которым осуществляется межклеточное взаимодействие, так называемые цитокины (иммунорегуляторы), а именно интерлейкин-2 и гамма-интерферон (белки, молекулы которых активируют иммунные клетки, атакующие пересаженный орган). Кроме этого, клетки Т-хел-перы выделяют другие медиаторы, интерлейкины-4,5, 6, которые запускают в В-лимфоцитах (клетках, производящих антитела) механизм выработки антител к трансплантату.
Медиаторы, выделяемые Т-лимфоцитами, вместе с комплементарными (взаимодополняющими) протеинами другой группы, участвующими в иммунных реакциях, - повреждают кровеносные сосуды нового органа, вызывая кровотечения, тромбозы, воспаления, омертвение и отторжение клеток. Обычно острое отторжение происходит в первые дни после пересадки органов. Хроническое отторжение - процесс, который наблюдается в течение многих месяцев или даже нескольких лет. Его главный признак - миграция и пролиферация (от латинского proles - отпрыск и fero - несу, увеличение числа клеток посредством клеточного деления (митоза), приводящее к росту ткани) гладкомышечных клеток в кровеносные сосуды трансплантата, постепенно блокирующие их. Постепенно в новом органе формируется рубцовая ткань, что нарушает его функцию.
Когда показана пересадка?
| Орган/Ткань | Фактор, ведущий к пересадке |
| Сердце | Сердечная недостаточность |
| Почки | Отказ почек |
| Легкие | Легочная гипертония, пузырьковый фиброз |
| Поджелудочная железа | Диабет |
| Тонкий кишечник | Синдром короткого кишечника |
| Роговица | Дегенерация |
| Костный мозг | Лейкемия |
| Кожа | Ожоги |
| Вены | Блокированные артерии (сердце, ноги) |
Подбор тканей и иммуноподавление
Для определения совместимости между донорским органом и тканями реципиента иммунологи проводят антигенный анализ тканей. После трансплантации риск отторжения снижается при помощи специальных препаратов.
Существует две стратегии минимизации эффекта отторжения: антигенный подбор до трансплантации и иммуноподавление после нее.
Антигенный анализ
Главный комплекс тканевой совместимости (ГКТС) - группа молекул, имеющаяся на поверхности всех клеток, которая распознается Т-лимфоцитами, запускающими механизм отторжения. В организме человека ген, отвечающий за работу ГТКС, находится в шестой хромосоме. ГТКС называют человеческим лейкоцитарным антигеном (ЧЛА, человеческие лейкоцитарные антигены - антигены тканевой совместимости, HLA, Human Leucocyte Antigens). ЧЛА подразделяются на два класса.
Молекулы ГТКС I класса подразделяются на А, В, С (примерно 80 молекул) и присутствуют на поверхности всех типов клеток, кроме эритроцитов.
Молекулы ГТКС II класса подразделяются на DR, DQ и DP (около 35 молекул) и находятся на поверхности антиген-представляющих клеток, например В-лимфоцитов.
Если бы удалось добиться совместимости 100% по ЧЛА между донором и реципиентом, как в случае с однояйцевыми близнецами, то все проблемы с отторжением трансплантируемых органов были бы ликвидированы. К сожалению, пока в реальности это недостижимый результат. Согласно исследованиям, хорошей считается совместимость по ЧЛА-DR (20 молекул), в этом случае гарантируется хорошая приживаемость трансплантированного органа. С целью проверить совместимость между донорским органом и организмом реципиента, проводятся следующие иммунологические тесты.
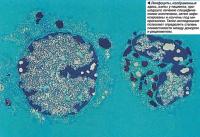
Лимфоциты (большая группа белых клеток крови) добавляются к группе антител ЧЛА-DR и находятся при комнатной температуре в течение 30 минут.
Иммунный белок, активируемый антителами, вызывающий гибель клеток, - добавляется к смеси и выдерживается 60 минут. Это уничтожает клетки, к которым присоединились антитела.
Краситель (например, эозин или трипановый синий) добавляется к смеси, затем следует фиксация (например, формалином).
Реакция проверяется при помощи специального светового микроскопа (фазово-контрастного). Мертвые клетки прокрашиваются. Когда этот тест проведен, для донора и реципиента это дает возможность принять решение о пересадке органов. При хорошей иммунной совместимости уровень приживаемости трансплантата составляет в течение года от 80 до 90% в зависимости от органа.
Жизнь после пересадки органов
Пациенты, перенесшие трансплантацию органов, в подавляющем большинстве возвращаются к активному образу. Однако до конца жизни они вынуждены принимать иммуноподавляющие препараты.
К сожалению, эти лекарства имеют побочные эффекты, такие как высокое кровяное давление, проблемы с почками, головная боль, тремор кистей и усиление роста волос.
Подавление иммунитета имеет и «другую сторону медали» - пациент становится чрезвычайно чувствительным к бактериальным, вирусным или грибковым инфекциям. Увеличивается и риск развития онкологических заболеваний.
Иммуноподавление
Главный принцип иммуноподавления состоит в блокировании механизмов отторжения имплантированных органов и тканей. Для иммуноподавления чаще всего используются три наиболее широко употребляемых препарата (так называемая тройственная терапия).
Циклоспорин А. Производное грибка, препарат подавляет выделение цитокининов из Т-хелпер-лимфоцитов и снижает уровень интерлейкина-2 у Т-цитотоксических лимфоцитов.
Азатиоприн. Останавливает пролиферацию лимфоцитов. Это предупреждает их фатальное действие.
Стероиды. Неспецифически подавляют воспаление, тормозя активацию макрофагов (клетки, способные к активному захвату и перевариванию токсичных для организма частиц и микроорганизмов) и уменьшая экспрессию ГКТС-антигенов.
После операции по пересадке органов или тканей дозы иммуноподавляющих препаратов меняются на основе биопсии (взятых на анализ образцов тканей) пересаженного органа. В настоящее время исследуются другие способы иммуноподавления, например, использование антител, направленных против определенных лимфоцитов, которые способны доставить токсичные препараты непосредственно к ним. Однако идеальным было бы иммуноподавляющее средство, которое только подавляло бы отторжение, не нанося вреда организму, но, к сожалению, такой препарат пока не создан.
Тело человека. Снаружи и внутри. №25 2008